Zakażenia kości należą do najtrudniejszych w terapii powikłań bakteryjnych, a ich leczenie od lat pozostaje wyzwaniem zarówno dla medycyny, jak i farmakologii. Nowe rozwiązanie opracowane przez polskich naukowców pokazuje, że przełom może przyjść z połączenia chemii, biologii i inżynierii materiałowej. Mikroskopijne „nanokwiaty” pozwalają dostarczać antybiotyk bezpośrednio do ogniska choroby, co zmienia sposób myślenia o leczeniu zapalenia kości i szpiku.
Dlaczego zapalenie kości jest tak trudne do leczenia
Osteomyelitis to choroba wywoływana najczęściej przez bakterie takie jak gronkowiec złocisty czy pałeczka ropy błękitnej. Drobnoustroje mogą kolonizować słabo ukrwione fragmenty tkanki kostnej oraz tworzyć biofilm – strukturę, która skutecznie chroni je przed działaniem antybiotyków i układu odpornościowego. W efekcie standardowa terapia wymaga wielotygodniowego podawania silnych leków w wysokich dawkach.
Problem polega na tym, że antybiotyki podawane ogólnoustrojowo docierają do kości w ograniczonym stopniu. Aby osiągnąć skuteczne stężenie, konieczne jest zwiększanie dawek, co prowadzi do obciążenia organizmu i ryzyka poważnych działań niepożądanych. W skrajnych przypadkach choroba prowadzi do martwicy kości, deformacji u dzieci lub konieczności amputacji.
Nanotechnologia inspirowana budową kości
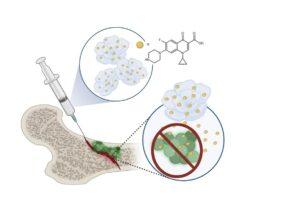
Zespół kierowany przez dr hab. Kamilę Sadowską z Instytutu Biocybernetyki i Inżynierii Biomedycznej PAN opracował nanostruktury przypominające kształtem kwiaty. Ich budowa nie jest przypadkowa – składają się z komponentu organicznego (białka, np. albuminy) oraz nieorganicznego (fosforanów metali), co odzwierciedla naturalną strukturę tkanki kostnej.
Takie podejście wpisuje się w szerszy nurt badań nad materiałami biomimetycznymi, które naśladują rozwiązania obecne w przyrodzie. Podobnie jak w czasach Mikołaja Kopernika, kiedy obserwacja natury prowadziła do przełomów w astronomii i matematyce, współczesna nauka wykorzystuje analogie między strukturą biologiczną a projektowanymi materiałami, aby zwiększyć skuteczność technologii medycznych.
W badaniach wykorzystano m.in. fosforan cynku, który sprzyja tworzeniu stabilnych struktur oraz zwiększa wydajność procesu ich powstawania. Wcześniejsze próby z udziałem miedzi okazały się mniej przydatne ze względu na jej toksyczność. Istotnym krokiem było także zastosowanie hydroksyapatytu – naturalnego składnika kości – co dodatkowo zwiększa zgodność materiału z organizmem.
Precyzyjne dostarczanie leków i nowe możliwości terapii
Kluczową innowacją jest zdolność nanokwiatów do przenoszenia antybiotyku bezpośrednio do miejsca zakażenia. W strukturę nośnika skutecznie wbudowano m.in. cyprofloksacynę, a badania laboratoryjne oraz testy na modelach zwierzęcych wykazały zahamowanie wzrostu bakterii przy jednocześnie niskiej toksyczności.
Mechanizm działania wpisuje się w jeden z najważniejszych kierunków współczesnej medycyny – terapię celowaną. Zamiast oddziaływać na cały organizm, lek trafia dokładnie tam, gdzie jest potrzebny. W przypadku kości ma to szczególne znaczenie, ponieważ ograniczone ukrwienie utrudnia dystrybucję substancji aktywnych.
Nanokwiaty pełnią jednocześnie podwójną funkcję. Oprócz transportu leku mogą wspierać regenerację tkanki kostnej dzięki swojej organiczno-mineralnej budowie. To połączenie działania przeciwbakteryjnego i wspomagania odbudowy wpisuje się w interdyscyplinarny charakter współczesnej nauki, łączącej medycynę, chemię i inżynierię materiałową.
Rozwijane w Polsce rozwiązanie pokazuje, że zaawansowane technologie medyczne mogą powstawać na styku wielu dziedzin – podobnie jak w dorobku Kopernika, gdzie matematyka, obserwacja i analiza prowadziły do nowych modeli rzeczywistości. W tym przypadku celem jest nie opis Wszechświata, lecz skuteczniejsze leczenie chorób, które dotąd pozostawały wyjątkowo oporne na terapię.





